Mekanisme Reaksi-Reaksi Adisi pada Aldehid dan Keton
Mekanisme Reaksi-Reaksi Adisi pada Aldehid dan Keton
Aldehid dan keton mempunyai rumus molekul sama, rumus umum CnH2nO.
Aldehida pada umumnya lebih reaktif terhadap substitusi nukleofilik jika dibandingkan dengan keton hal tersebut karena elektronik dan juga efek sterik. Atom hidrogen pada aldehid yang relatif kecil melekat pada satu sisi gugus karbonil, gugus R yang lebih besar ditempelkan pada sisi lainnya. Pada keton, gugus R melekat di dua sisi ggus karbonil. sehingga, hambatan sterik lbih sedikit di aldehid daripada di keton.
Reaksi Adisi merupakan reaksi pemutusan ikatan rangkap.
Karbonil nya bersifat polar, karenanya dapat diserang atau dimasuki oleh nukleofilik (Nu:-) ataupun diserang atau dimasuki oleh elektrofilik (E+)
Reaksi umum
Ada beberapa faktor yang dapat mrmprngaruhi reaktivitas aldehid atopun keton :
1. Fator sterik
2. Muatan (+) pada karbon karbonil
3. Faktor elektronik karena adanya resonansi
Reaktivitas Naik
Reaksi-reaksi adisi aldehid dan keton
1. Reksi Adisi Air (H2O) atau Penambahan air
Penambahan air ke hasil aldehida dalam pembentukan hidrat.
Pembentukan hidrat berlangsung melalui mekanisme adisi nukleofilik.
1) Air, bertindak sebagai nukleofil, tertarik pada karbon sebagian positif dari gugus karbonil, menghasilkan ion oksonium.
1) Air, bertindak sebagai nukleofil, tertarik pada karbon sebagian positif dari gugus karbonil, menghasilkan ion oksonium.
2) Ion oksonium membebaskan ion hidrogen yang diambil oleh anion oksigen dalam reaksi asam-basa.
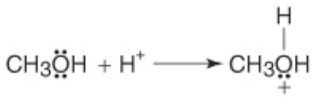
Sejumlah kecil asam dan basa mengkatalisasi reaksi ini. Ini terjadi karena penambahan asam menyebabkan protonasi oksigen dari gugus karbonil, yang mengarah pada pembentukan muatan positif penuh pada karbon karbonil, menjadikan karbon sebagai inti yang baik. Menambahkan ion hidroksil mengubah nukleofil dari air (nukleofil lemah) menjadi ion hidroksida (nukleofil yang kuat). Keton biasanya tidak membentuk hidrat stabil.
2. Reaksi adisi alkohol (R-OH) atau Penambahan alkohol
Reaksi aldehida dengan alkohol menghasilkan hemiasetal atau asetal. Mencampur dua reaktan bersama menghasilkan hemiasetal. Mencampur dua reaktan dengan asam klorida menghasilkan asetal. contohny, reaksi metanol dengan ethanal menghasilkan hasil seperti ini.
Substitusi nukleofilik dari gugus OH untuk ikatan rangkap gugus karbonil membentuk hemiasetal melalui mekanisme berikut ini:
1) Pasangan elektron yang tidak terbagi pada atom oksigen alkohol menyerang gugus karbonil.
2) Hilangnya ion hidrogen ke anion oksigen menstabilkan ion oksonium yang terbentuk pada Langkah 1.
Penambahan asam ke hemiasetal menciptakan asetal melalui mekanisme berikut:
1) Proton yang dihasilkan oleh disosiasi asam klorida memprotonasi molekul alkohol dalam reaksi asam-basa.
2) Pasangan elektron yang tidak terbagi dari oksigen hidroksil dari hemiasetal menghilangkan proton dari alkohol yang terprotonasi.
3) Ion oksonium hilang dari hemiasetal sebagai molekul air.
4) Molekul kedua alkohol menyerang karbon karbonil yang membentuk asetal terprotonasi.
5) Ion oksonium kehilangan proton ke molekul alkohol, membebaskan asetal.
3) Reaksi adisi hidrogen sianida (HCN) atau Penambahan hidrogen sianida
ke gugus karbonil dari aldehida atau sebagian besar keton menghasilkan sianohidrin bisa juga disebut sebagai hidroksinitril. Namun, keton yang terhalang secara statis, tidak mengalami reaksi ini. Mekanisme penambahan hidrogen sianida adalah penambahan nukleofilik langsung di ikatan oksigen karbonil karbonil.
ke gugus karbonil dari aldehida atau sebagian besar keton menghasilkan sianohidrin bisa juga disebut sebagai hidroksinitril. Namun, keton yang terhalang secara statis, tidak mengalami reaksi ini. Mekanisme penambahan hidrogen sianida adalah penambahan nukleofilik langsung di ikatan oksigen karbonil karbonil.
4. Reaksi adisi reagen organologam atau Penambahan reagen organologam
Pereaksi Grignard, senyawa organolitium, dan natrium alkinida bereaksi dengan formaldehida untuk menghasilkan alkohol primer, semua aldehida lain untuk menghasilkan alkohol sekunder, dan keton untuk menghasilkan alkohol tersier
Referensi
https://www.cliffsnotes.com/study-guides/chemistry/organic-chemistry-ii/aldehydes-and-ketones/reactions-of-aldehydes-and-ketones
Permasalahan
1. Mengapa Aldehida biasanya lebih reaktif terhadap substitusi nukleofilik jika dibandingkan dengan keton?
2. Pasa reaksi adisi air mengapa Keton umumnya tidak membentuk hidrat stabil?
3. Mengapa karbonil yang ada pada aldehid dan keton dapat di serang oleh nukleofilik ataupun elektrofilik?
https://www.cliffsnotes.com/study-guides/chemistry/organic-chemistry-ii/aldehydes-and-ketones/reactions-of-aldehydes-and-ketones
Permasalahan
1. Mengapa Aldehida biasanya lebih reaktif terhadap substitusi nukleofilik jika dibandingkan dengan keton?
2. Pasa reaksi adisi air mengapa Keton umumnya tidak membentuk hidrat stabil?
3. Mengapa karbonil yang ada pada aldehid dan keton dapat di serang oleh nukleofilik ataupun elektrofilik?



















Komentar ini telah dihapus oleh pengarang.
BalasHapusSaya Wafiqah Alvia Ramadhani (047) akan menjawab Permasalahan no. 1
BalasHapusAldehida lebih reaktif daripada keton, karena aldehid memiliki atom hidrogen yang dibutuhkan pada gugus karbonilnya. Hal tersebut menyebabkan aldehid sangat mudah teroksidasi. Sedangkan keton tidak memiliki atom hidrogen sehingga tidak mudah dioksidasi.
Selain itu ada lagi yang menjadi penentu mengapa aldehid lebih reaktif daripada keton :
◈ Hambatan sterik aldehida lebih kecil dibandingkan keton (atom hidrogen lebih kecil dari gugus organik lainnya).
◈ Karbon karbonil dalam aldehida umumnya memiliki muatan parsial positif dibandingkan gugus alkil dengan sifat pendonor-elektronnya. Aldehida hanya memiliki satu gugus penyumbang-elektron sedangkan keton memiliki dua gugus.
Terimakasih, semoga bermanfaat 😊
Komentar ini telah dihapus oleh pengarang.
BalasHapusWISLIANA A1C118060
BalasHapus3. Karbonil yang ada pada aldehid dan keton dapat di serang oleh nukleofilik ataupun elektronik dikarenakan karbonil bersifat polar sehingga dapat diserang leh nukleofilik atau pun elektronik. Untuk rinciannya begini.
Atom oksigen pada gugus karbonil C=O jauh lebih elektronegatif dibanding karbon sehingga memiliki kecenderungan kuat untuk menarik elektron2 yang ada dalam ikatan C=O ke arahnya sendiri. Salah satu dari 2 pasang elektron yg membentuk ikatan rangkap C=O bahkan lebih mudah tertarik ke arah oksigen. Ini yang menyebabkan ikatan rangkap C=O sangat polar. Oleh karena itu, karbon karbonil bersifat elektrofilik, sehigga lebih reaktif terhadap nukleofil . Sehingga karbonil yang ada pada aldehid dan keton dapat diserang oleh nukleofil ataupun elektrofilik.
Assalamu'alaikum wr wb, perkenalkan saya Nurhalimah (A1C118024) disini saya akan mencoba menjawab permasalahan no 2 dimana permasalahan nya yaitu Pasa reaksi adisi air mengapa Keton umumnya tidak membentuk hidrat stabil?
BalasHapusSebelumnya disini saya saya sedikit mengomentari permasalahan saudari Nadiya dimana saudari nadiya disini tidak memberikan reaksi konkritnya dimana hal tersebut dikarenakan kesetabilan suatu senyawa hidrat ditentukan oleh ada atau tidaknya rantai samping yang menyebarkan muatan positif dari gugus karbonil. Sehingga jika ada reaksinya lebih dapat diketahui kesetabilan senyawa hidrat tersebut. Selain itu hal itu juga dikarenakan keton tidak mempunyai sifat mereduksi seperti aldehid karena pada gugus karbonilnya (—CO) tidak mengandung atom H.